

Organ
der
GD — Gesellschaft für Dermopharmazie e.V.
| Home |
| Ausgabe: 1/2016 |
| 1/2015 |
| 1/2014 |
| 1/2013 |
| 1/2012 |
| 2/2011 |
| 1/2011 |
| 1/2010 |
| 1/2009 |
| 1/2008 |
| 2/2007 |
| 1/2007 |
| 2/2006 |
| 1/2006 |
| 2/2005 |
| 1/2005 |
| 2/2004 |
| 1/2004 |
| 2/2003 |
| 1/2003 |
| 2/2002 |
| 1/2002 |
| 4/2001 |
| 3/2001 |
| 2/2001 |
| 1/2001 |
| 1/2000 |
| Weitere Links: |
| Gesellschaft für Dermopharmazie |
 |
|
Ausgabe März 2001 |
Dermatotherapie
Dermatotherapeutika am Horizont
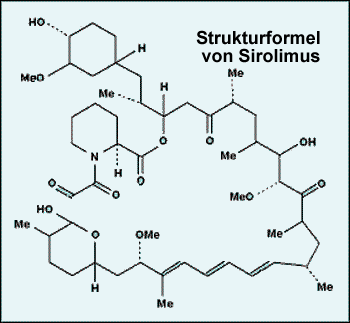
Sirolimus
Bei diesem auch als Rapamycin bekannten Makrolid handelt es sich um ein Stoffwechselsubstrat des Pilzes Streptomyces hygroscopicus. Es wurde bereits vor zwanzig Jahren im Rahmen eines Antibiotika-Screenings durch die Ayerst Research Laboratories entdeckt, aber trotz seiner Wirksamkeit gegen Hefepilze jahrelang in keiner Indikation verwendet. Das änderte sich erst, als das strukturell sehr ähnliche, erst einige Jahre später entdeckte Tacrolimus zur Behandlung der Transplantatabstoßung und neuerdings auch zur Behandlung der atopischen Dermatitis verwendet wurde.
 Beim
Einsatz in der Transplantationsmedizin macht man sich die Suppression von
T-Lymphozyten durch Makrolide zunutze, die dann das Spendergewebe nicht
mehr angreifen. Die Indikationserweiterung wurde durch die Erkenntnis eingeleitet,
dass auch bei der atopischen Dermatitis eine überaktivität von T-Zellen
im Rahmen allergischer Reaktionen auftritt. Für Sirolimus konnte der immunsuppressive
Effekt anhand eines verminderten Einbaus von radioaktiv markiertem Phosphor
in Hefe- RNA- und -DNA- Stränge nachgewiesen werden. Man erhofft sich nun
eine ähnlich starke Wirksamkeit und gute Verträglichkeit wie bei Tacrolimus
inklusive der Einsatzmöglichkeit bei atopischer Dermatitis.
Beim
Einsatz in der Transplantationsmedizin macht man sich die Suppression von
T-Lymphozyten durch Makrolide zunutze, die dann das Spendergewebe nicht
mehr angreifen. Die Indikationserweiterung wurde durch die Erkenntnis eingeleitet,
dass auch bei der atopischen Dermatitis eine überaktivität von T-Zellen
im Rahmen allergischer Reaktionen auftritt. Für Sirolimus konnte der immunsuppressive
Effekt anhand eines verminderten Einbaus von radioaktiv markiertem Phosphor
in Hefe- RNA- und -DNA- Stränge nachgewiesen werden. Man erhofft sich nun
eine ähnlich starke Wirksamkeit und gute Verträglichkeit wie bei Tacrolimus
inklusive der Einsatzmöglichkeit bei atopischer Dermatitis.In den letzten Jahren wurde der Wirkmechanismus von Tacrolimus und Sirolimus aufgeklärt. Er unterscheidet sich von dem der Glucocorticoide, was vermuten lässt, dass bei der Anwendung weitaus weniger Nebenwirkungen auftreten könnten. Der Angriffspunkt ähnelt dem eines dritten sehr gängigen und effektiven, aber nebenwirkungsreichen Immunsuppressivums, dem zyklischen Oligopeptid Ciclosporin. Sowohl Sirolimus als auch Tacrolimus sind lipophil genug, um ohne Carriervermittlung in das Zytoplasma ihrer Zielzellen zu permeieren. Hier konkurrieren sie um denselben zytosolischen Rezeptor. Diese Zielstruktur zählt zur Gruppe der sogenannten Makrophiline (also der ”Makrolid-liebenden" Rezeptoren) und wird als Sirolimus-Tacrolimus-bindendes Protein bezeichnet. Nur als Komplex sind beide Makrolide in der Lage, in den Zellkern einzuwandern.
| Unter der überschrift "Dermatotherapeutika am Horizont" stellen wir Ihnen in loser Folge das pharmakologische Profil von Stoffen vor, die eines Tages Einzug in die Dermatotherapie halten könnten. Den Anfang macht das Makrolid Sirolimus, das aufgrund seiner immunsuppressiven Eigenschaften Hoffnungen auf Anwendbarkeit bei atopischer Dermatitis und anderen allergischen Hauterkrankungen weckt. Die Ausführungen über Sirolimus stammen aus der Feder von Apothekerin Bettina Sauer, Doktorandin von Professor Dr. Monika Schäfer-Korting am Fachbereich Pharmazie der Freien Universität Berlin. |
Tacrolimus inhibiert nun die calciumabhängige Serin-Threonin-Kinase Calcineurin, die normalerweise Transkriptionsfaktoren der Interleukin-(IL)-Synthese aktiviert. Der Tacrolimus-induzierte IL-2-Mangel hemmt die Proliferation und Aktivierung von T-Lymphozyten. Zellzyklusanalysen ergaben, dass Tacrolimus letztlich den übergang der T-Lymphozyten von der G0-Phase, das heißt der inaktiven Ruheform, zur wieder proteinsynthetisierenden und in Folge letztlich mitosebereiten G1-Phase verhindert.
Der Sirolimus-Makrophilin-Komplex stattdessen bindet nicht an Calcineurin, sondern an ein anderes, ganz neu entdecktes Ziel, nämlich das mTOR (mammalian Target of Rapamycin). Hierbei handelt es sich ebenfalls um eine Serin-Threonin-Kinase, deren Hemmung auch mit einer Senkung der T-Lymphozytenaktivität korreliert. Im Zellzyklus wird durch Sirolimus der übergang von der G1- zur S-Phase, also von der Proteinbiosynthese zur DNA-Replikation, blockiert. Obgleich der Zellzyklus demnach an verschiedenen Stellen unterbrochen ist, bleibt als Ergebnis beider Pharmaka eine in Bezug auf allergische Hauterkrankungen vielversprechende T-Zell-Inaktivierung. Ferner normalisieren beide Makrolide erhöhte IgE-Spiegel, wie sie bei atopischer Dermatitis vorliegen.
Die Erwartungen an Sirolimus steigen, da sich Tacrolimus auch bei breiter lokaler Anwendung als gut verträglich erwiesen hat. Allerdings müssen klinische Studien mit Sirolimus noch erfolgen und bestätigen, dass bei topischer Anwendung wirklich nur die erhoffte Dämpfung überschießender Immunreaktionen auftritt, nicht aber eine schädliche Unterdrückung der körpereigenen Abwehr. Außerdem sind zum Ausschluss systemischer Nebenwirkungen Blutspiegeluntersuchungen erforderlich.
Sind klinische Studien erfolgreich, wird das Interesse an beiden Pharmaka voraussichtlich noch weiter steigen und über die oben aufgeführten Indikationen hinausgehen. Aufgrund des Wirkmechanismus von Sirolimus und Tacrolimus erhofft man sich nämlich auch eine Anwendbarkeit bei Alopecia areata, Lupus erythematodes und Lichen ruber.
Literatur
Abraham et al., Immunopharmakology of Rapamycin, Annu. Rev. Immunol. 14, 483-510 (1996) Brattstrom et al., Pharmacokinetics and safety of single oral doses of sirolimus in healthy male volunteers, Ther. Drug Monit. 22 (5), 537-544 (2000)
Ingle et al., Sirolimus: Continuing the evolution of transplant immunosuppression, Annl. Pharmacother 34, 1044-1055 (2000)
nach oben